
点击右上角![]() 微信好友
微信好友
 朋友圈
朋友圈

请使用浏览器分享功能进行分享

日前,元化智能科技骨科手术机器人系统正式获得由英国标准协会(BSI)颁发的欧盟MDR证书,取得进军欧盟及全球市场的“绿色通行证”。
欧盟医疗器械MDR法规于2021年正式全面实施,是目前全球医疗器械领域监管要求最为严格的认证之一,也是产品进入欧盟市场、贴附CE标志的核心前提。相比旧版MDD指令,新法规在临床证据要求、上市后监督、产品可追溯性及独立第三方公告机构审查等方面均大幅提升了标准,是进入欧盟市场的强制性法律要求。
未获此证书的产品,将无法在欧盟27国及全球众多认可CE标志的国家销售,也无法通过欧盟海关或在欧洲医院进行招标采购。此次颁证机构英国标准协会(BSI)由英国王室特许授权,是全球最权威的认证机构之一,其签发的MDR证书在全球医疗器械行业具有极高公信力。能够顺利通过BSI审核并获得MDR认证,意味着企业在设计开发、生产制造、风险管理和上市后监控等全链条均达到了欧盟的严苛要求。
据介绍,元化智能科技成立于2018年,专注于高端专科智能医疗装备的创新研发与精密智造。历经7年耕耘,公司成长为国内唯一拥有骨科手术机器人全部核心部件自主研发能力的企业,形成了覆盖术前规划、术中导航、耗材配套、术后康复的全周期产品布局。多年来,从产品研发阶段的设计控制、风险管理,到生产过程中的过程验证、无菌保障,再到上市后的警戒体系、临床随访,每一个环节均对标欧盟最高标准,实现体系化的质量管理。
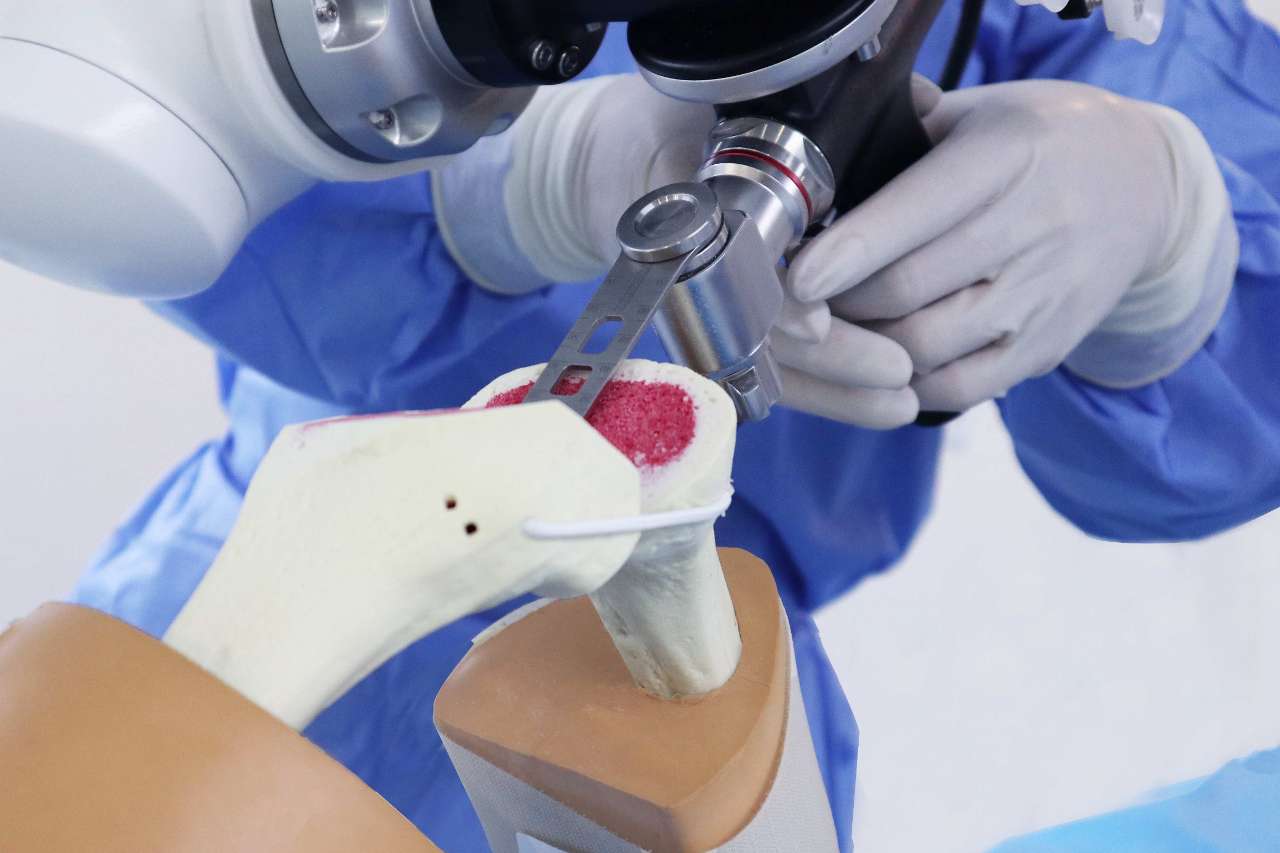
2025年,元化智能在一年内斩获12张国内外医疗器械注册认证,覆盖手术机器人“设备—软件—耗材—康复”全流程,引发国内外医疗器械业界的高度关注。此前,公司已相继取得巴西、东南亚等国家和地区的产品注册许可,此次欧盟MDR认证,是这一系列国际化布局中分量最重的一步。
欧盟是全球第二大医疗器械市场,规模超千亿欧元,且准入门槛极高。此次证书的获得,意味着元化智能已具备向欧盟成员国申请产品CE认证的资质,为旗下骨科手术机器人产品进入欧洲医院打通了制度通道。
此外,欧盟MDR认证在全球范围内的“溢出效应”同样不可忽视。亚太、中东、非洲及拉丁美洲众多国家在制定本国医疗器械准入政策时,均将EU MDR认证作为重要参考依据甚至直接互认条件。因此,这张证书不仅是进入欧洲的“通行证”,更将大大加速元化智能在全球其他市场的准入进程,形成国际化布局的“乘数效应”。
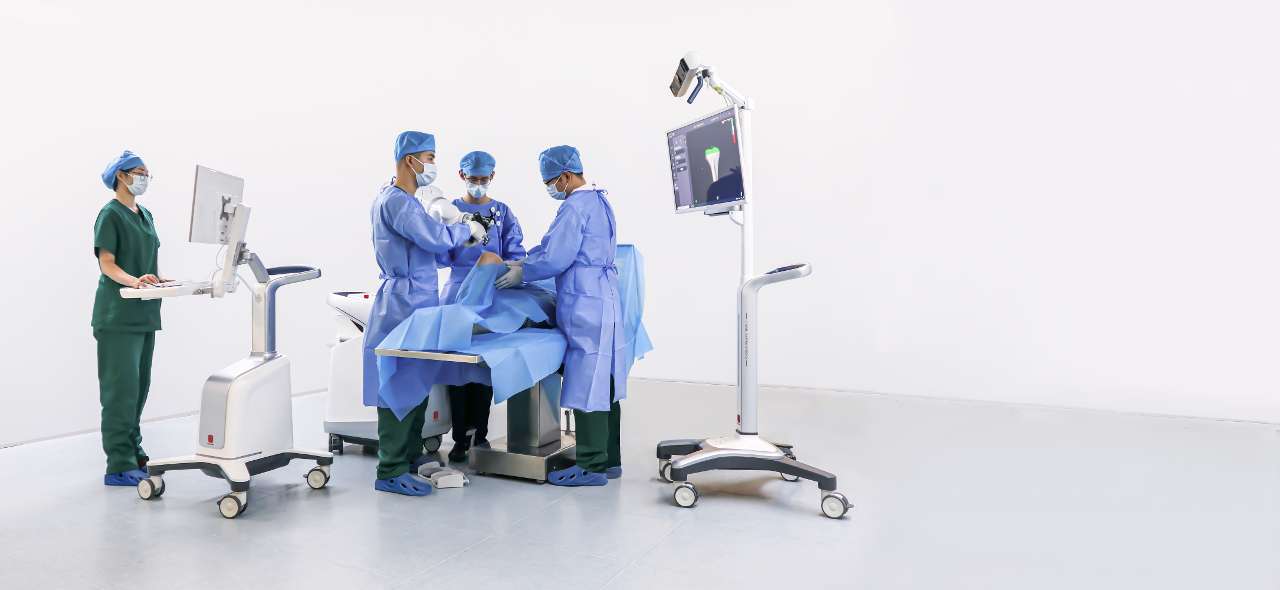
长期以来,高端手术机器人市场被国际巨头把持,核心技术受制于人。元化智能以自主创新为根基,7年完成了从0到1、从1到N的蜕变——不仅打破了国际垄断,更以持续的认证积累向世界宣示:中国品牌完全有能力登上全球高端医疗器械的竞技舞台。
从深圳出发,从国家药监局三类证到BSI颁发的EU MDR认证,元化智能的每一步都在扩展着中国智造医疗装备的全球版图,书写着属于中国高端医疗机器人的新篇章。
元化智能董事长、创始人孟李艾俐表示,此次获得MDR认证,推动企业建立起一套"设计有依据、生产有控制、出货有记录、售后有监控"的闭环管理系统,实现了组织能力的全面重塑——不仅意味着获得了与国际一线医疗器械巨头同台竞技的资格,更意味着企业已构建起全球化高质量发展的战略基石。
【深看工作室】
审稿人:严圣禾
编校:钟欢欢
